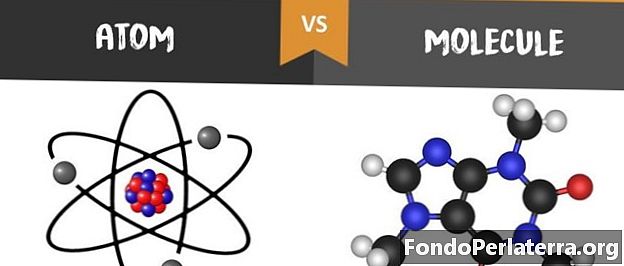
Atomas prieš molekulę

Turinys
- Turinys: skirtumas tarp atomo ir molekulės
- Palyginimo diagrama
- Kas yra „Atom“?
- Kas yra molekulė?
- Pagrindiniai skirtumai
- Vaizdo įrašo paaiškinimas
Pagrindinis atomo ir molekulės skirtumas yra tas, kad atomas yra sudarytas iš neutronų, protonų ir elektronų, o molekulė reiškia atomų grupę, sujungtą tarpusavyje kovalentiniu arba joniniu metalu.
Turinys: skirtumas tarp atomo ir molekulės
- Palyginimo diagrama
- Kas yra „Atom“?
- Kas yra molekulė?
- Pagrindiniai skirtumai
- Vaizdo įrašo paaiškinimas
Palyginimo diagrama
| Išskyrimo pagrindas | Atomas | Molekulė |
| Apibrėžimas | Atomas reiškia mažiausią elementų dalelę, kurioje yra elemento savybės | Molekulės reiškia atomų grupę arba atomų derinius |
| Priklausomybė | Gali arba negali | Taip |
| Medžiagos savybės | Gali arba negali | Taip |
| klasifikacija | Ne | Du: homo- ir heteroatomi |
| Stiprumas | Pagrindiniai materijos elementai | Žmogaus kūne yra daugiau molekulių nei visatos žvaigždžių |
| Egzistavimas | Ji negali egzistuoti savarankiškai | Jis gali egzistuoti savarankiškai |
| Pavyzdžiai | Deguonis, vandenilis ir azotas | H2, NO ir kt. |
Kas yra „Atom“?
Atomas - tai mažiausias paprastosios medžiagos dalelių vienetas, turintis cheminio elemento savybes. Visų rūšių dujos, kietos medžiagos, skysčiai ir plazma yra sudaryti iš jonizuotų arba neutralių atomų. Paprastai jie yra labai maži ir negali būti matomi plika akimi ir didinamuoju mikroskopu. Atomo dydis gali būti apie dešimt milijardo metro. Aš kalbu apie jų ribas, tada jos neturi tiksliai apibrėžtų ribų.
Palaipsniui tobulėjant fizikai, į atominius modelius buvo įtraukti kvantiniai principai, kurie paaiškina geresnį ir numatomą atomo elgesį. Kiekvienas atomas, sudarytas iš vieno ar daugiau elektronų, sujungtų su branduoliu.
Atomo branduolys yra sudarytas iš vieno ar daugiau protonų ir paprastai turi panašų neutronų skaičių. Atomo branduolys taip pat yra apsuptas elektronų, kurie yra neigiamai įkrautos dalelės. Atomas gali būti neigiamai arba teigiamai įkrautas, priklausomai nuo daugumos dalelių. Kai šie neigiami ar teigiami atomai susilieja, sudarydami molekules, jungtis suformuoja elektronai, užpildydami išorines atomų orbitas. Atome nėra jungimosi, nes atomai egzistuoja nepriklausomai.

Kas yra molekulė?
Molekulė yra mažiausia elektriškai neutralios grupės dalelė, kurioje yra to junginio ar elemento cheminės savybės. Juos sudaro atomai, kuriuos palaiko cheminiai ryšiai. Jie visiškai skiriasi nuo jonų, nes neturi elektros krūvio.
Daugelio cheminių medžiagų atomai greitai jungiasi su kitais atomais, sudarydami molekules. Jų dydis ir sudėtingumas gali skirtis. Jie visada juda. Skysčiuose ir kietose medžiagose jie yra sandariai supakuoti. Kietosios būsenos jų judesį galima palyginti su greita vibracija. Skystos būsenos jos laisvai juda viena kitos atžvilgiu savotiškai slinkdamos. Dujų būsenoje jų tankis yra mažesnis, palyginti su kietu ir skystu to paties cheminio ryšio ryšiu, ir juda dar laisviau, palyginti su skysčiu.
Palyginti su atomu, molekulė turi savybę egzistuoti vien dėl to, kad atome yra elektronas. Molekulėje atomas gali būti stabilus tik tuo atveju, jei yra pakankamai elektronų. Remiantis kinetine dujų teorija, „molekulė dažnai naudojama bet kuriai dujinei dalelei, nepaisant jos sudėties. Dėl monoatominės molekulinės struktūros kietųjų dujų atomai taip pat laikomi molekulėmis. “

Pagrindiniai skirtumai
- Atomas yra mažiausia elemento dalelė, o molekulė yra mažiausia junginio dalelė.
- Atomas gali egzistuoti arba ne egzistuoti nepriklausomai, o molekulė visada egzistuoja nepriklausomai.
- Atomas gali turėti arba neturi materijos savybių, o molekulė visada turi materijos savybes.
- Molekulės yra sudarytos iš atomų atomo, kurį sudaro neutronai, protonai ir elektronai.
- Atomas gali būti molekulė dėl nepriklausomos egzistencijos. Atomai yra monoatominėje molekulėje dėl stabilumo veiksnių, tokių kaip tauriosios dujos ir helis, tuo tarpu molekulė negali pasakyti, kad atomas.
- Atomai neturi kitų rūšių, tuo tarpu dviejų rūšių molekulės yra homoatominės ir heteroatominės
- Atomai visiškai nesieja, o molekulės turi tarpmolekulines jėgas ir vidines molekulės
- Atomų išdėstymas gali būti matomas rentgeno spinduliais, o molekulėse sąveika leidžia žmogui judėti, jausti, daugintis ir daug kitų dalykų.
- Trys skirtingi atomo tipai yra vandenilio atomas, deuterio atomas ir tritis. Dviejų tipų molekulės yra paprasta molekulė ir sudėtinga molekulė.
- Atomas negali egzistuoti savarankiškai, o molekulė gali egzistuoti nepriklausomai.
- Elemento atomas negali gyventi laisvoje būsenoje, o molekulės gali gyventi laisvoje būsenoje.
- Atomo masės praktiškai neįmanoma nustatyti, o atskirų atomų masių suma sudaro molekulės masę.
- Atomai gali įgyti ir prarasti elektronus, sudarydami jonus, o molekulės negali įgyti ar prarasti elektronų, sudarydami jonus.
- Neįmanoma pamatyti atomo per plika akimi ir net per didinamąją molekulę. Molekulės taip pat negalima pamatyti plika akimi, bet ją galima pamatyti per labai didinantį mikroskopą.
- Atomas negali būti toliau dalijamas, o molekulė gali būti toliau dalijama, kad būtų atskiri atomai.
- Atomas turi branduolinę trauką arba jungiasi su ja, o molekulė turi cheminį trauką arba ryšį tarp atomų.