Kovalentinės obligacijos ir joninės jungtys

Turinys
- Turinys: Kovalentinių ir joninių jungčių skirtumas
- Palyginimo diagrama
- Kas yra kovalentinės obligacijos?
- Kas yra joninės jungtys?
- Pagrindiniai skirtumai
Pagrindinis skirtumas tarp joninių ir kovalentinių jungčių yra elektronų porų ir atomų pasidalijimas. Kovalentinėse jungtyse atomai elektrostatiškai traukiami vienas kito atžvilgiu, tuo tarpu jonų jungtyse; elektronų poros pasidalija tarp atomų.
Turinys: Kovalentinių ir joninių jungčių skirtumas
- Palyginimo diagrama
- Kas yra kovalentinės obligacijos?
- Kas yra joninės jungtys?
- Pagrindiniai skirtumai
- Vaizdo įrašo paaiškinimas
Palyginimo diagrama
| Išskyrimo pagrindas | Kovalentinės obligacijos | Joninės jungtys |
| Apibrėžimas | Kovalentinis ryšys yra tam tikros rūšies cheminė jungtis, kuri apima dalijimąsi poromis arba jungimosi poras (elektronų poras) tarp atomų. | Joninis ryšys yra cheminės jungties rūšis, apimanti vieno ar daugiau elektronų pasidalijimą arba visišką atidavimą vienu atomu į kitą atomą. |
| Atsiradimas | Kovalentiniai ryšiai yra neutralių atomų sąveikos rezultatas | Joninės jungtys yra anijonų ir katijonų sąveikos rezultatas. |
| Cheminis potencialas | Tai gana silpni cheminiai ryšiai | Tai yra stipriausias cheminių jungčių tipas. |
| Formavimas | Nemetaliniai elementai sudaro kovalentinius ryšius | Metaliniai elementai sudaro jonines jungtis |
| Elektronų būsena | Bendri elektronai | Bendras elektronų perkėlimas |
| Medžiagos padėtis | Skysčiai ir dujos kambario temperatūroje | Kietos dalelės kambario temperatūroje |
| Junginiai | Ekologiški | Neorganinis |
| Tirpumas | Netirpus vandenyje | Tirpus vandenyje |
| Figūra | Neabejotina forma | Nėra apibrėžtos formos |
| Pavadinimas | Graikų kalbos priešdėliai | Romos skaitmenys |
| Pavyzdžiai | Vandenilio chlorido rūgštis ir metanas | Sieros rūgštis ir natrio chloridas |
Kas yra kovalentinės obligacijos?
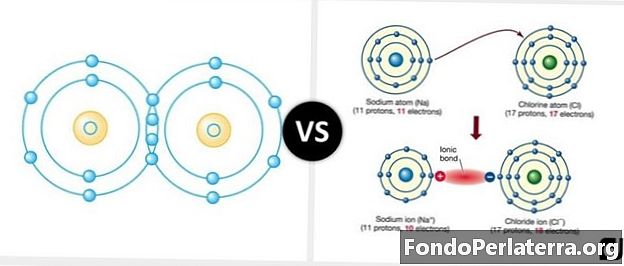
Kovalentiniai ryšiai, dar vadinami molekulinių jungčių pavadinimu, yra cheminių ryšių rūšis, kuri apima dalijimąsi poromis arba jungimosi poras (elektronų poras) tarp atomų. Daugumoje molekulių elektronai, pasidalijantys, leidžia kiekvienam atomui gauti viso išorinio apvalkalo ekvivalentą, atitinkantį stabilią elektroninę konfigūraciją. Jei atomai turi panašų afinitetą elektronams, tikėtina, kad įvyks kovalentiniai ryšiai dėl to paties afiniteto elektronams ir nėra linkę juos dovanoti atomai. Atomai dalijasi elektronais, kad gautų okteto konfigūraciją ir taptų stabilesni ir stipresni. Dėl sigmos ir pi orbitalių sąveikos kovalentiniai ryšiai gali sudaryti keturių tipų jungtis: viengubas, dvigubas, trigubas ir keturgubas. Deguonies atomai yra geriausias pavyzdys, reikalaujantis dviejų papildomų elektronų, kad susidarytų uždaras apvalkalas, o vandenilio atomų - vieno, kad būtų sudarytas uždaras apvalkalas. Deguonies atomas dalijasi du savo elektronus su vandenilio atomais, taigi abiejų atomų korpusai yra uždari. Tai galiausiai sukuria vandens molekulę.
Kas yra joninės jungtys?
Joninis ryšys yra cheminės jungties rūšis, apimanti vieno ar daugiau elektronų pasidalijimą arba visišką atidavimą vienu atomu į kitą atomą. Joninės jungtys yra tų elementų, kurie lengvai praranda elektronus, ir tų elementų, kurie įgyja elektronus, rezultatas. Šios rūšies jungtys visiškai nėra skirtos molekulėms dėl krūvių sąveikos, kaip aprašyta Kulono įstatyme. Joninės jungtys kambario temperatūroje išlieka kietos, nes periodiškai susidarant milteliams su milijardais jonų, kiekvienas jonas yra apsuptas daugybe priešingo krūvio jonų. Elektrostatiniai atotrūkiai tarp neigiamų ir teigiamų jonų sulaiko junginį kartu. Bendra energija joninio jungimosi metu paprastai yra teigiama, tai rodo, kad reakcija yra endoterminė ir nepalanki. Kita vertus, ši reakcija tuo pačiu metu yra palanki dėl jų elektrostatinės traukos. Dažnas joninės jungties pavyzdys yra natris arba druska. Natrio atomai greitai suteikia elektronus, kurie lemia teigiamą krūvį. Chloras priima šiuos elektronus ir neigiamai įkrauna. Šie du priešingai įkrauti atomai tada pritraukia vienas kitą, kad sudarytų natrio chlorido molekulę.
Pagrindiniai skirtumai
- Kovalentinėse jungtyse elektronų orbitos sutampa, o joninių jungčių atveju jos yra atskiros.
- Kovalentiniai ryšiai yra gana minkšti, palyginti su joninėmis jungtimis, kurios yra kietos ir trapios.
- Tiek metalo atomai, tiek nemetalo atomai dalyvauja formuojant joninius ryšius, o formuojant kovalentinius ryšius; dalyvauja tik nemetalų atomai.
- Kovalentiniai ryšiai susidaro dėl dalijamųjų elektronų, o joniniai ryšiai susidaro dėl elektronų perkėlimo.
- Molekulės yra kovalentinių ryšių dalelės junginio susidarymo metu, tuo tarpu joniniuose ryšiuose tai yra teigiamai įkrauti ir neigiamai įkrauti jonai.
- Kovalentinės jungtys nėra laidininkai, o joninės jungtys yra laidininkai.
- Kovalentinis ryšys vyksta tarp atomų, kurių elektronegatyvumas mažai skiriasi. Jonų ryšys vyksta tarp atomų, turinčių didelį skirtumą tarp elektronegatyvumo.
- Joninės jungtys reikalauja aukšto lydymosi ir virimo taško, jei joninės jungtys. Kovalentiniai ryšiai reikalauja žemos lydymosi ir virimo temperatūros, jei kovalentinis ryšys.
- Metanas ir druskos rūgštis yra dažni kovalentinio natrio chlorido ir sieros rūgšties pavyzdžiai.
- Kovalentinės jungtys turi apibrėžtą formą, tuo tarpu joninės jungtys neturi apibrėžtosios
- Kovalentinės jungtys turi mažą poliškumą, tuo tarpu joninės jungtys turi aukštą poliškumą.
- 100% kovalentinės molekulės ištirps aliejuje, bet ne vandenyje, o daugelis joninių jungčių gali ištirpti vandenyje, bet ne aliejuje.
- Kovalentiniai ryšiai yra svarbūs, nes anglies molekulės sąveikauja pirmiausia kovalentiniu ryšiu, o joninės jungtys yra svarbios, nes jos leidžia sintetinti specifinius organinius junginius.
- Kovalentiniai ryšiai gali būti tiek elementai, tiek junginiai, o joniniai ryšiai gali būti tik junginiai.