Absorbcija ir adsorbcija
Turinys
- Turinys: absorbcijos ir adsorbcijos skirtumas
- Kas yra absorbcija?
- Kas yra adsorbcija?
- Pagrindiniai skirtumai
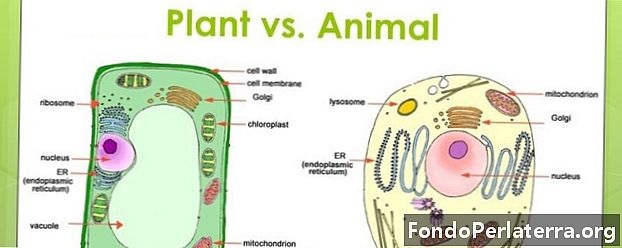
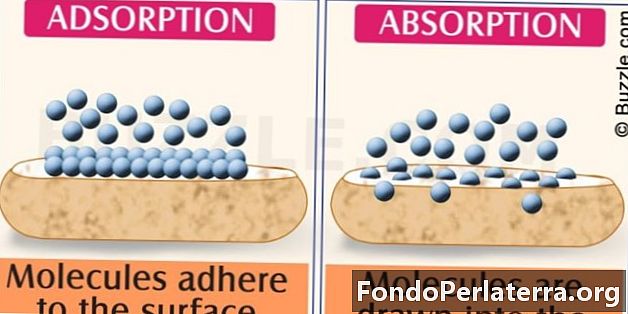
Pagrindinis skirtumas tarp absorbcijos ir adsorbcijos yra absorbcija - tai procesas, kurio metu skystis ištirpinamas kietu arba skystu. Adsorbcija, atvirkščiai, yra procesas, kurio metu jonai, molekulės ar atomai iš tokios medžiagos kaip dujos, kieti ar skysti, prilimpa prie adsorbento paviršiaus.

Turinys: absorbcijos ir adsorbcijos skirtumas
- Kas yra absorbcija?
- Kas yra adsorbcija?
- Pagrindiniai skirtumai
- Vaizdo įrašo paaiškinimas
Kas yra absorbcija?
Absorbcija yra procesas, kurio metu viena medžiaga visiškai patenka į kitą. Tai procesas, kurio metu vienas atomas ar molekulė išsiurbiama iš kitų molekulių tūrio. Tai turi būti medžiagos dalis, visiškai į ją įeinant. Tai gali būti cheminis ar fizinis procesas. Pavyzdžiui, anglies dioksidas gali būti absorbuojamas į kalio karbonato tirpalą. Tai yra cheminės absorbcijos pavyzdys, nes vyksta reakcija. Kitas pavyzdys galėtų būti oro ištirpinimas vandenyje. Tai fizinė absorbcija, nes oras į pusiausvyros slėgį patenka į vandens vidų. Kai kuri nors medžiaga ar medžiaga absorbuoja tam tikrą skysčio ar dujų kiekį viduje, tada sakoma, kad ta medžiaga absorbavo kitą medžiagą. Taigi, absorbuojamas, kažkas juda medžiagos viduje.
Kas yra adsorbcija?
Adsorbcija yra procesas, kurio metu dujos ar skystis nėra absorbuojamas, o susidaro tik paviršiuje. Dėl sintetinių priežasčių ir vandens valymo, adsorbcijos reiškinys yra plačiai naudojamas pramonėje. Tai apima sukibimą. Šiame procese cheminė medžiaga tiesiog priglunda prie kitos medžiagos, neįeidama į jos vidų. Pavyzdžiui, anglies dioksidas yra ant adsorbento paviršiaus slėgio svyruojančio adsorbento vieneto viduje, jis yra ant kieto adsorbento paviršiaus.
Pagrindiniai skirtumai
- Molekulinių rūšių įsisavinimas visoje birių kietų ar skystų medžiagų medžiagoje yra absorbcija. Molekulinių rūšių kaupimasis paviršiuje ir nepatekimas į jį yra vadinamas adsorbcija.
- Absorbcija yra didelis reiškinys, o adsorbcija - paviršiaus reiškinys.
- Absorbcija yra endoterminis procesas, o adsorbcija - egzoterminis procesas.
- Temperatūra neturi įtakos absorbcijai, o žemai temperatūrai - adsorbcijai.
- Absorbcija vyksta vienoda sparta, tuo tarpu adsorbcijos greitis stabiliai didėja, o galiausiai pasiekia pusiausvyrą.
- Koncentracija yra absorbcija yra vienoda visoje medžiagoje. Koncentracija ant paviršiaus skiriasi adsorbcija nei didžioji dalis.
- Absorbcija komerciškai naudojama aušintuvuose ir vandens valymui.
- Absorbcija yra susijusi su tūriu, o adsorbcija - su paviršiumi.
- Absorbcija apima ištirpimą ir difuziją, o adsorbcija - sukibimą.
- Sugeriant, fotono energiją sugeria kitas subjektas.